
「ケトン食が新たながん治療の選択肢となる可能性も出てきました」と語る萩原圭祐さん
がんになると、それまでの食事を見直す人は多い。ただ、何を食べれば、再発を防げるか、また進行・再発がんに対してどういった食事がいいのか、現時点では確固たるエビデンス(科学的根拠)は存在しないのが現状のようだ。そうした中、新たな可能性として注目されているのがケトン食。進行・再発がんに著しく有効だったという研究結果が明らかとなった。化学療法などと併用した新たな治療法として注目されている。
「これを食べれば」は存在しない
がん患者に対するケトン食の有用性を明らかにしたのは、大阪大学大学院医学系研究科漢方医学寄附講座准教授の萩原圭祐さんらの研究グループ。
萩原さんによると、がんと食事の関係は、大まかにいってがんになっていない人(予防のための食事)、がんになり手術・化学療法・放射線療法を受けた人(再発予防のための食事)、進行・再発した人(進行抑制のための食事)と、がんの状態によってそれぞれ分けて考えるべきだという。
がん予防と食事との関係については、国立がん研究センターが行った長期にわたる疫学研究「多目的コホート研究」の結果が報告されている。この研究の結果からは、高塩分食や野菜不足がわずかにがんのリスクを高めることがわかったが、「これを食べればがんにならない」といった特定のがん予防食品やサプリメント、食事療法は今のところ存在しないという。
また、がんになった人に対する食事療法・栄養療法の有効性についても、「欧米での研究も含め、現在のところ『この食事ががんに効く』といったような、効果を示せるものはありません」と萩原さんは語る。
「がんと食事」でわかったこと
それでも、予防も含め、がんと食事の関係で意外なことが明らかになりつつある。例えば、がんと脂肪との因果関係だ。
「一般的には脂肪分の過剰摂取が大腸がんや乳がんの最大のリスク因子といわれてきました。しかし、米国で行われた約5万人の閉経女性を対象とした8年間の追跡調査の結果、脂肪摂取は大腸がん、乳がんの発症リスクとはいえないことが報告されました」
そこで改めて注目されているのが、極北に生きるイヌイットの食習慣だ。過酷な環境で暮らすイヌイットは総摂取エネルギーのうち40%を超える形で脂肪を摂取し、低炭水化物・高脂肪食を摂っている。ところが、急性心筋梗塞、多発性硬化症、糖尿病などの罹患率はデンマーク人と比べて低く、がん患者の発生率も極めて低い。ただ、がん患者の発生率が低かったのは、伝統的な食習慣である低炭水化物・高脂肪食が守られている間で、1910年以降、欧米型の食文化が入り、40年が経過した1950年代からは、欧米型のがん(大腸がん、肺がん、乳がん、前立腺がん)が増加しているという。
つまり、イヌイットの食習慣から考えられることは、十分な脂肪摂取と共に、低炭水化物つまり糖質を控える食生活が、がんの発生を減らしているのではないかということなのである。
糖質とがんとの関係明らかに
糖質を摂取すると分泌されるインスリンとがんとの関係についての報告もある。
厚生労働省研究班がCペプタイド値(インスリンがどの程度膵臓から分泌されているか調べるための値で、値が高いほどインスリン分泌量が多い)と大腸がんリスクとの関係を調べた結果、Cペプタイド値が高い男性は低い男性に比べて最大で3倍も大腸がんになりやすかった。
乳がんになりやすいようにしたモデルマウスを使った実験では、一般食を投与した場合は1年で50%のマウスが乳がんを発症するのに対して、糖質を減らした低炭水化物・高タンパク質食を投与した群では、発がんが有意に減少した。
そこで萩原さんは語る。「こうした結果から糖質の過剰摂取と発がんとの関係が推測され、人でも糖質を制限した高脂肪食の効果が報告されるようになりました。例えば、65歳の女性の悪性膠芽腫患者に抗がん薬・放射線療法と併用して糖質制限・高脂肪食を摂ってもらったところ、がんが縮小し、有効だったことが報告されています」
そこで萩原さんたちが考えたのが、がん患者に対する糖質制限・高脂肪食、つまりケトン食の導入だった。
糖質制限・高脂肪食であるケトン食
ケトン食とは食事療法の1つで、糖質の摂取を極端に減らして、かわりにタンパク質と脂肪分を多く摂る食事法のこと。十分な栄養が摂れず飢餓状態になったとき、体内で作られエネルギー源となるのが脂肪酸の代謝産物であるケトン体だ。
通常、体内では糖質が主要なエネルギー源となっている。ところが、食事ができないなど何らかの理由で糖質が枯渇すると、代わりに脂肪が分解されてケトン体が作られ、これをエネルギー源として利用することができる(図1)。私たちの体に備わっているこの仕組みを利用したのがケトン食だ。
図1 体内でケトン体が産生される仕組み(概略図)
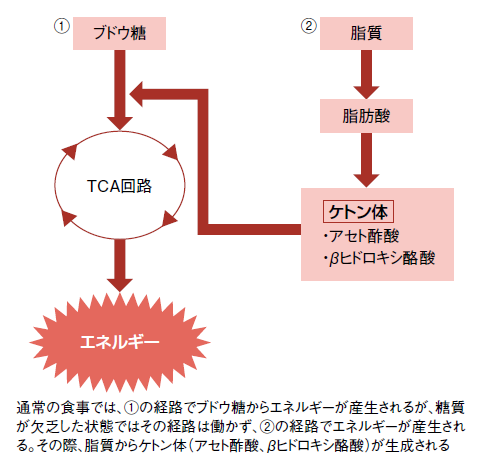
萩原さんによると、ヒポクラテスの時代から絶食がてんかんの発作を減らすことは知られていたそうだ。絶食によって一時的に飢餓状態にして糖質を枯渇させ、その結果、体内では脂肪からケトン体が作られ、糖質に変わるエネルギー源となるのだ。
1921年、米国で絶食よりも負担の少ない方法としてケトン食が考案され、難治性てんかん患者に用いられて劇的な発作軽減効果があることが示された。日本でもてんかん発作を抑える治療の1つとして取り入れられており、大阪大学医学部附属病院の小児科では、難治性てんかんやGlut1欠損症に対して15年間のケトン食の実績があるという。
従来は主として難治性てんかん患者に用いられたケトン食が、萩原さんはがん治療、中でも進行・再発したがんにも有効ではないかと考えた。大阪大学ゲノム審査委員会の承認を得て、日本人のがん患者に対するケトン食の有用性と安全性を検討することを目的に、2013年2月から介入研究を開始、その結果を2015年10月に発表した。
]]>




